全面揭示各種碳環與富勒烯之間獨特的pi-pi相互作用!
全面揭示各種碳環與富勒烯之間獨特的pi-pi相互作用!
Comprehensively revealing the unique pi-pi interactions between different cyclocarbon and fullerene!
文/Sobereva@北京科音 2024-Oct-28
0 前言
18碳環以其獨特的幾何和電子結構,自從2019年在凝聚相觀測到后引發了化學界的巨大關注。與之相關的分子間相互作用文章已有不少,例如《全面探究18碳環獨特的分子間相互作用與pi-pi堆積特征》(http://www.shanxitv.org/572)介紹的Carbon, 171, 514-523 (2021)、《8字形雙環分子對18碳環的獨特吸附行為的量子化學、波函數分析與分子動力學研究》(http://www.shanxitv.org/674)介紹的Phys. Chem. Chem. Phys., 25, 16707 (2023)、《理論設計新穎的基于18碳環構成的雙馬達超分子體系》(http://www.shanxitv.org/684)介紹的Chem. Commun., 59, 9770 (2023),等等。筆者迄今對18碳環及其衍生物的研究論文匯總和各種相關博文見http://www.shanxitv.org/carbon_ring.html(不斷更新)。
碳單環體系和富勒烯體系是碳元素的兩種關鍵的同素異形體,形狀截然不同,一個環形一個球形,而且由于二者都有pi共軛特征,理應存在pi-pi相互作用。這顯著的差異性和明顯的共性無疑使得碳環與富勒烯的相互作用非常值得進行細致、充分的探索。近期,北京科音自然科學研究中心(http://www.keinsci.com)的盧天和江蘇科技大學的劉澤玉在知名的Chem. Eur. J.(歐洲化學)期刊上發表了極為全面、系統、透徹的研究不同尺寸碳環(C18到C36)與不同數目C60富勒烯相互作用的理論研究文章,充分揭示了它們之間獨特的相互作用,包括強度、結構和本質,內容很新穎有趣,非常歡迎閱覽和引用:
Zeyu Liu, Tian Lu*, Theoretical Insight into Complexation Between Cyclocarbons and C60 Fullerene, Chem. Eur. J., 30, e202402227 (2024) DOI: 10.1002/chem.202402227
可以通過此鏈接免費在線閱覽:https://onlinelibrary.wiley.com/share/author/PJDSJZN8IMBAVDCCBXQS?target=10.1002/chem.202402227
此文不僅研究碳環與富勒烯相互作用本身,文章在分析思想和方法學方面對于其它分子間相互作用的研究也頗有借鑒意義,十分推薦對這類研究問題感興趣的讀者閱讀。此文充分運用了強大的Multiwfn(主頁http://www.shanxitv.org/multiwfn)波函數分析程序提供的豐富的弱相互作用分析功能,包括IGMH、sobEDA、范德華勢等,是Multiwfn研究弱相互作用問題的很好的范例。Multiwfn支持的弱相互作用分析功能在《Multiwfn支持的弱相互作用的分析方法概覽》(http://www.shanxitv.org/252)有概述,在量子化學波函數分析與Multiwfn程序培訓班(http://www.keinsci.com/workshop/WFN_content.html)的“弱相互作用的分析”部分有最全面透徹的講解和演示。
下面將對上述Chem. Eur. J.文章的主要內容進行深入淺出的介紹,便于讀者更容易理解文章的研究結果,同時額外附上許多分析和計算細節以幫助讀者能夠將文中的研究手段舉一反三運用到自己的研究中。原文里還有很多細節信息和討論,故請閱讀下文后閱讀原文。
1 碳環-富勒烯二聚體
文章首先考察了碳環與富勒烯形成的二聚體結構。文中用Gaussian 16在ωB97XD/6-311G*級別下優化了碳環Cn (n=18, 20, 22, 24, 26, 30, 32, 34, 36)與富勒烯形成的二聚體C60@Cn,并確認了無虛頻。ωB97XD泛函曾用于http://www.shanxitv.org/carbon_ring.html里羅列的筆者的各種18碳環的研究中,不僅可以正確描述18碳環的幾何結構(見Carbon, 165, 468 (2020)中的方法對比測試),也能合理描述弱相互作用,故很適合用于優化涉及碳環的復合物。得到的二聚體中比較有代表性的5個如下所示。可以看到隨著碳環尺寸的增大,富勒烯逐漸陷入碳環中,到了C60@C34的時候富勒烯正好不偏不倚精確嵌入在碳環的正中央,富勒烯的中心和碳環的中心正好重合,這是一個完美的納米土星(nano-saturn)結構。而當碳環尺寸進一步增大到C36,為了最大化分子間相互作用,富勒烯的中心自發偏離了碳環的中心。
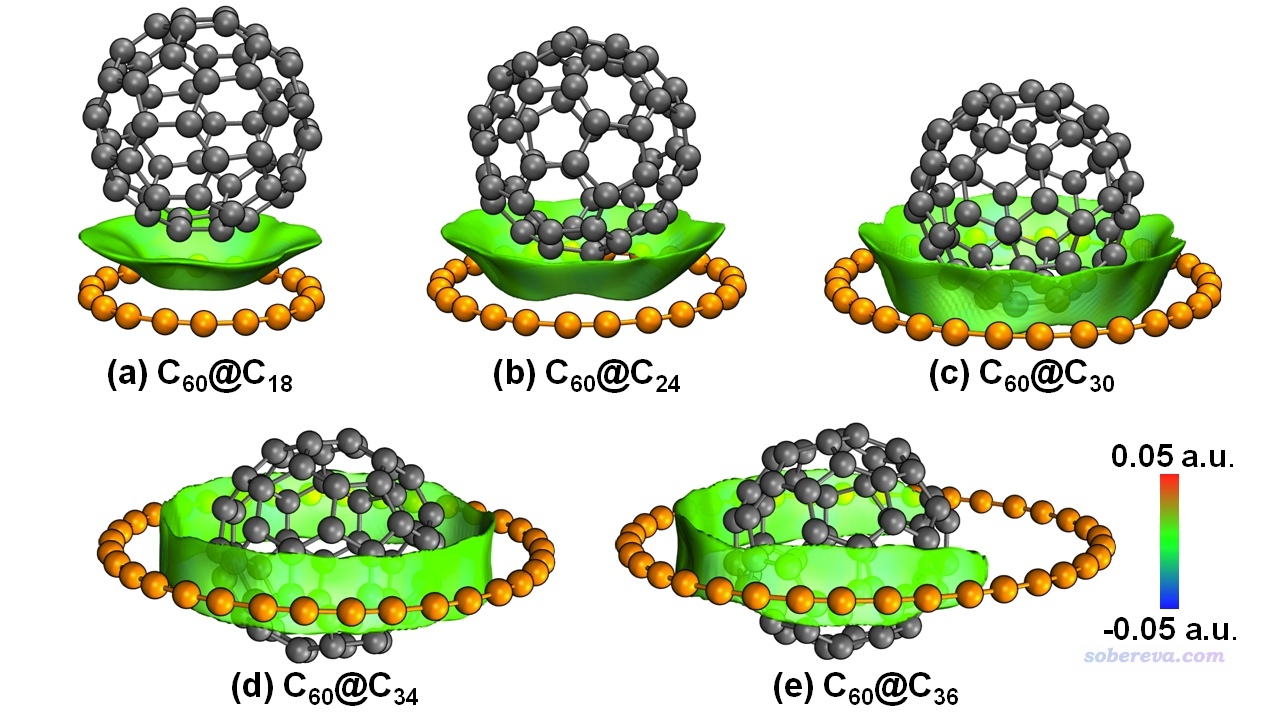
筆者提出的IGMH是目前非常流行、效果理想的可視化片段間相互作用的分析方法,見《使用Multiwfn做IGMH分析非常清晰直觀地展現化學體系中的相互作用》(http://www.shanxitv.org/621)和《一篇最全面介紹各種弱相互作用可視化分析方法的文章已發表!》(http://www.shanxitv.org/667)介紹的綜述。上圖的等值面是IGMH方法定義的sign(λ2)ρ著色的δg_inter等值面,描述富勒烯和碳環這兩個片段間的相互作用。圖中非常清楚直觀地展現出了碳環-富勒烯之間的相互作用區域。等值面幾乎都是綠色,說明相互作用區域的電子密度數值非常低,pi-pi相互作用區域普遍具有這種特點,再加上碳環和富勒烯的接觸面也正是pi電子分布的區域相互接觸,無疑富勒烯和碳環之間的結合是典型的pi-pi相互作用所驅動的。
為了嚴格考察碳環和富勒烯的結合強度,基于Gaussian優化的幾何結構,文中用ORCA程序精確計算了不同碳環與富勒烯形成二聚體對應的結合能,即E_bind = E(C60@Cn) - E(C60) - E(Cn),其中E是電子能量,每個能量都在各自分別優化的結構下得到。計算級別用的是ωB97M-V/def2-QZVPP,ωB97M-V不僅像ωB97XD一樣是長程極限HF成份為100%的范圍分離泛函因而能夠合理描述碳環的電子結構,而且大量測試都體現了其計算弱相互作用能相當優秀,在《簡談量子化學計算中DFT泛函的選擇》(http://www.shanxitv.org/272)中以及北京科音中級量子化學培訓班(http://www.keinsci.com/workshop/KBQC_content.html)里的“弱相互作用的計算與相關問題”專題部分也專門說過這一點。def2-QZVPP是相當高質量的基組,算分子間相互作用能的BSSE問題小到可以忽略,在ORCA里利用RIJCOSX加速技術計算像C60@C36這樣約100個非氫原子體系的單點能完全算得動。此外,為了從熱力學角度嚴格考察C60@Cn二聚體形成的可能性,文中還計算了標況下的結合自由能,其中對電子能量的自由能熱校正量通過《使用Shermo結合量子化學程序方便地計算分子的各種熱力學數據》(http://www.shanxitv.org/552)介紹的Shermo程序基于ωB97XD/6-311G*振動分析的輸出文件得到。如552博文所述,像這種含有大量很低頻的體系的自由能的計算一定要用Shermo支持的quasi-RRHO模型得到的自由能熱校正量,而切勿直接用Gaussian等程序基于RRHO模型給出的,否則低頻模式對熵的貢獻可能被高估得離譜,導致結合自由能誤差很大。另外,為了考察溶劑效應對結合的影響,文章還使用Gaussian的SMD溶劑模型按照《談談隱式溶劑模型下溶解自由能和體系自由能的計算》(http://www.shanxitv.org/327)說的做法獲得了水環境下的自由能,并求差得到了水中的結合自由能。計算結果匯總如下
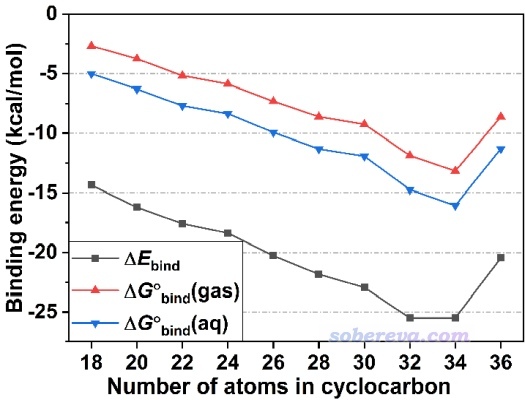
由上圖可見,從C18到C32,隨著碳環尺寸的增大,它與富勒烯的結合強度近乎嚴格地線性增強,這是由于二者間的接觸面積逐漸增大,這點從上文的IGMH圖的等值面面積的變化就可以清晰地反映出來。而從C34變成C36,結合強度反倒減弱了,這正如IGMH圖所示的,C36有的地方與富勒烯離得相對較遠、作用較弱,導致δg_inter等值面也沒有在相應區域出現。
上圖體還現出標況氣相的結合自由能和基于電子能量算的結合能的變化趨勢基本一致,但前者沒有后者那么負,這是因為結合過程中熵減小對結合造成了嚴重不利的影響。對比上圖中的紅線和藍線可見水溶劑環境下的結合自由能比氣相下的更負幾kcal/mol,說明極性溶劑會促使碳環與富勒烯的結合,這本質上就是疏水效應,眾所周知疏水效應會驅動非極性物質間在水中的結合。
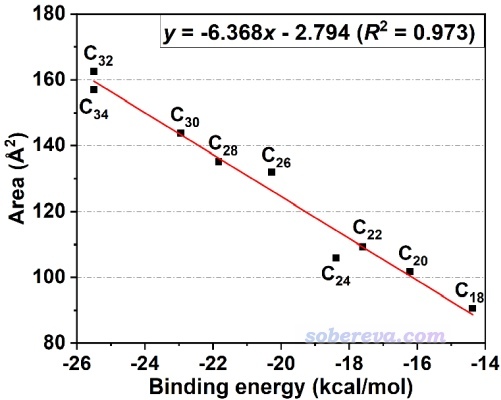
很值得一提的是,文中發現碳環-富勒烯之間的δg_inter=0.002 a.u.的等值面面積與它們的結合能有頗好的線性關系,如下所示。因此IGMH圖像的等值面面積在某些情況下可以作為解釋或預測相互作用能的很好的描述符,這一點很值得在未來進一步探索。這種面積的計算方法見《計算IGMH等值面的面積和體積的方法》(http://www.shanxitv.org/738)。
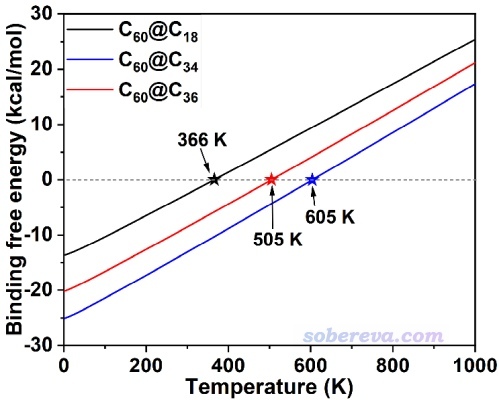
為了考察溫度對碳環-富勒烯結合的影響,以及探索結合的臨界溫度,文中利用Shermo程序做了自由能隨溫度的掃描,并進而得到了結合自由能與溫度的關系,如下所示。可見溫度越高越不利于結合,在氣相常壓下,C18碳環與富勒烯之間從366 K開始就無法結合了,而C34和富勒烯之間的二聚體在高達605 K以下都是可以形成的。C36的情況處于二者之間。
碳環與富勒烯的復合勢必造成單體的結構變化,由于單體結構相對于極小點結構改變導致單體的電子能量在復合過程中的升高稱為變形能。文中補充材料里的表S1給出了不同碳環與富勒烯結合時的碳環的變形能,發現C18到C34的變形能都<=0.3 kcal/mol,可以忽略不計,而C36的變形能則達到了1.0 kcal/mol,這一方面是因為這樣較大的碳環有足夠顯著的柔性,另一方面在于它與富勒烯之間的不對稱的相互作用(如全面IGMH圖所展示的),這造成了這種碳環在復合物中相對于圓形的極小點結構的不可忽略的形變。下圖是按照《在VMD中計算RMSD衡量兩個結構間的差異以及疊合兩個結構》(http://www.shanxitv.org/290)的方法繪制的C36在孤立狀態(紅線)和與富勒烯結合狀態(藍線)的疊加圖,可見富勒烯的存在誘使C36碳環被拉長了。

碳環與富勒烯的作用雖然形式上屬于“弱相互作用”類別,但結合強度真不是一般的強,而是相當的強!如《透徹認識氫鍵本質、簡單可靠地估計氫鍵強度:一篇2019年JCC上的重要研究文章介紹》(http://www.shanxitv.org/513)所列舉的,像是水二聚體這樣的一般強度氫鍵的結合能才-5 kcal/mol左右,而本文研究的與富勒烯結合最弱的18碳環,它與富勒烯的結合能都達到了-14.4 kcal/mol,將近三個普通氫鍵的強度。而且這比《全面探究18碳環獨特的分子間相互作用與pi-pi堆積特征》(http://www.shanxitv.org/572)提到的曾經筆者研究的兩個18碳環間的結合能-9.2 kcal/mol強得多,也比J. Chem. Theory Comput., 13, 274 (2017)高精度計算的兩個富勒烯之間的結合能-8.3 kcal/mol強得多!
2023年筆者提出的能量分解方法sobEDA和sobEDAw的詳細介紹見《使用sobEDA和sobEDAw方法做非常準確、快速、方便、普適的能量分解分析》(http://www.shanxitv.org/685),其中sobEDAw用于考察碳環+富勒烯的相互作用成份極為合適,速度足夠快而且結果也很準確。sobEDAw只對部分泛函擬合了參數,由于碳環體系需要HF成份較高的泛函才能正確描述,因此文中使用了HF成份達到50%的BHandHLYP泛函結合DFT-D3(BJ)色散校正和6-311+G(2d,p)基組做碳環-富勒烯之間的sobEDAw能量分解,并且考慮了counterpoise校正,結果是總相互作用能為-12.0 kcal/mol,其中靜電貢獻-8.4、交換互斥貢獻25.6、軌道相互作用貢獻-2.4、色散作用貢獻-26.8 kcal/mol。可見色散作用對碳環-富勒烯之間的吸引作用起絕對主導效果,靜電作用相對次要,而軌道相互作用可忽略不計。這完全符合pi-pi堆積的典型特征,在《全面探究18碳環獨特的分子間相互作用與pi-pi堆積特征》(http://www.shanxitv.org/572)介紹的Carbon, 171, 514 (2021)中使用sSAPT0/jun-cc-pVDZ級別對18碳環的pi-pi作用形成的二聚體做能量分解基本上也是這個情況。
此文還使用Multiwfn通過筆者提出的ADCH原子電荷計算方法,以及很常用的Mulliken方法,計算了C60@C18中18碳環部分的片段電荷。如果對原子電荷缺乏了解的話建議閱讀《一篇深入淺出、完整全面介紹原子電荷的綜述文章已發表!》(http://www.shanxitv.org/714)里提到的筆者的原子電荷綜述。這兩種方法給出的18碳環的電荷分別為0.015和-0.027,都十分接近于0,體現出碳環與富勒烯之間的基態的電荷轉移效應可以忽略不計。文中也用Multiwfn的主功能9的選項-1將18碳環和富勒烯分別定義成片段1和片段2,然后計算了它們之間的總Mayer鍵級,數值僅為可忽略的0.041,即基本沒有共享電子作用,再次體現出兩個分子間完全是非共價相互作用。如果讀者對鍵級不了解,建議看《Multiwfn支持的分析化學鍵的方法一覽》(http://www.shanxitv.org/471)中鍵級的相關部分。
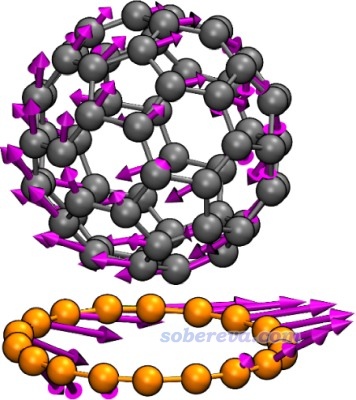
文中發現18碳環和富勒烯實際上有兩種極小點結構(見原文圖S1),次低的比最低的能量高0.9 kcal/mol,它們之間互變的過渡態的虛頻為9.8i cm-1,振動模式如下所示,可見明顯對應于富勒烯相對于18碳環的旋轉。在ωB97M-V/def2-QZVPP級別下計算出的正向和逆向勢壘分別為0.90和0.04 kcal/mol,極低的勢壘體現出復合物中富勒烯可以非常自由地旋轉。實際上pi-pi堆積作用的體系之間普遍容易發生滑移(如18碳環二聚體,在http://www.shanxitv.org/572里做了動力學模擬直接體現了這一點),因為滑移造成的能量變化很小。
2 碳環-富勒烯 2:1三聚體
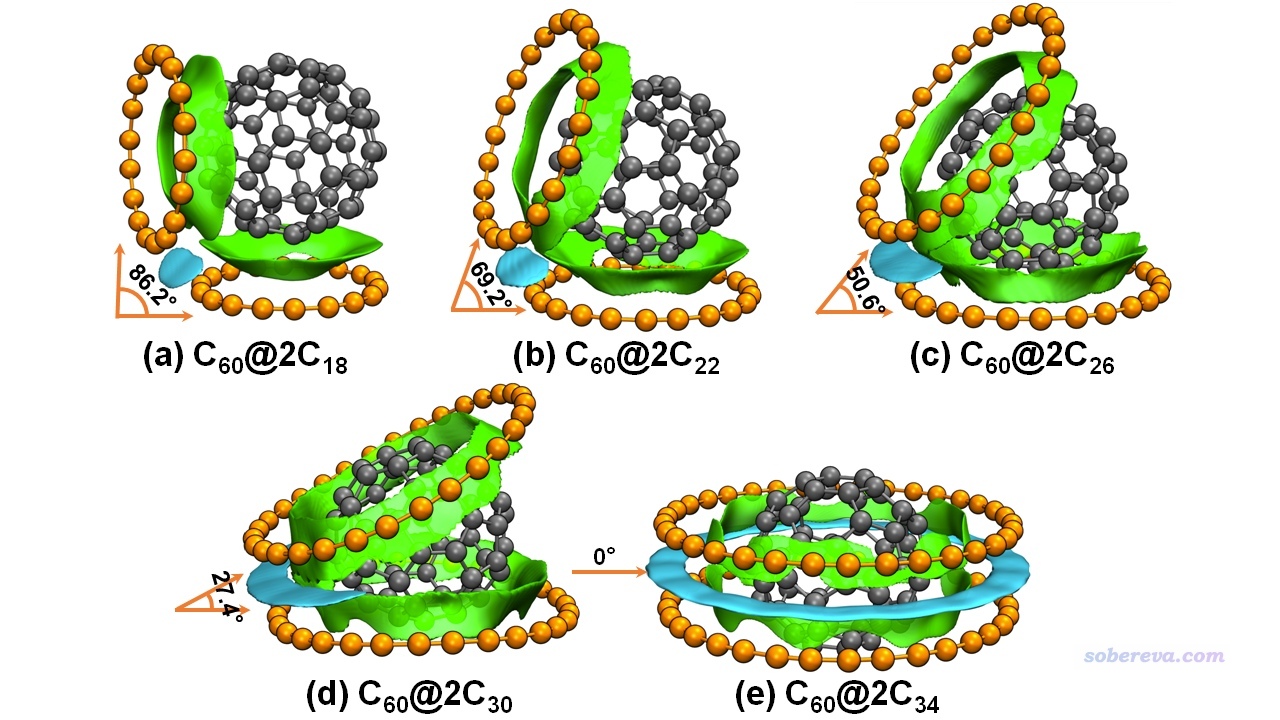
文章系統考察了一個富勒烯結合兩個碳環(C18至C34)形成的三聚體的結構,優化得到的結果如下圖所示。這種體系中既有碳環與富勒烯之間的相互作用,也有兩個碳環之間的相互作用,為了能直觀區分,這兩類相互作用的δg_inter等值面分別用綠色和青色著色,這樣的IGMH圖真是巨直觀!可以看到,隨著碳環的增大,兩個碳環間的夾角逐漸減小,富勒烯越來越多地被兩個碳環“吃”了進去,富勒烯始終與碳環保持著緊密的接觸和充分的pi-pi作用。當碳環大到C34時,兩個碳環之間完全平行并形成了全面的pi-pi相互作用,而且和http://www.shanxitv.org/572提到的18碳環二聚體一樣是較長的C-C鍵對著較短的C-C鍵,此時富勒烯已精確嵌入到了兩個碳環的正中間。
ωB97M-V/def2-QZVPP計算遠超100個非氫原子的體系時過于昂貴,因此文中在計算三聚體和更多聚體時在ORCA里使用的是ωB97M-V/def2-TZVP結合gCP方式的經驗性的BSSE校正,精度比ωB97M-V/def2-QZVPP差不了多少而耗時低得多得多。使用ωB97M-V/def2-TZVP+gCP,文中計算了富勒烯結合第一個碳環的結合能ΔE_1_bind,以及在此基礎上再結合第二個碳環的結合能ΔE_2_bind(即C60@Cn與Cn形成C60@2Cn的結合能),總的結合能(三聚體結合能)為ΔE_1_bind與ΔE_2_bind之和。結果如下圖(a)所示。可見隨著碳環增大,結合能越來越負、結合作用越來越強,而且ΔE_2_bind比ΔE_1_bind明顯更負,這體現出多個碳環與富勒烯結合的非常明顯的協同作用。如上面的IGMH圖所示,已有的一個碳環可以和另一個碳環形成pi-pi作用,而且碳環越大時pi-pi作用越顯著(青色等值面越來越大),這是為什么碳環越大時協同效應越強。
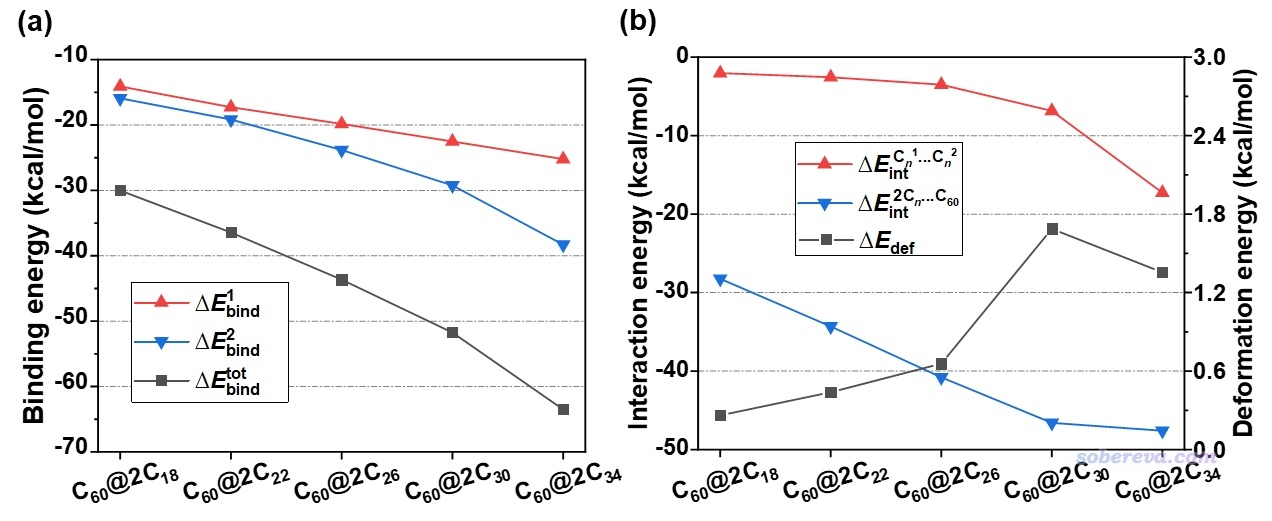
為了更進一步考察三聚體結構中不同片段之間的相互作用強度,此文還基于優化后的三聚體結構計算了片段間的相互作用能,如上圖(b)所示,兩個碳環間的相互作用能對應紅線,兩個碳環與富勒烯之間的相互作用能對應藍線。可見隨著碳環增大,碳環間的相互作用逐漸增強,特別是兩個C34碳環之間的相互作用格外強,這是因為如前面的IGMH所示,它們能形成完整的遍及整個碳環的pi-pi作用,而不再只是局部區域的pi-pi作用。還可見從C18到C30之間,碳環越大,由于可以和富勒烯相互作用的原子越多,碳環-富勒烯的相互作用越強,但是從C30到C34這種相互作用反倒稍微變弱了,這是因為在C60@2C34中C34與富勒烯的接觸不像C60@2C30中C30與富勒烯的接觸那么充分,這一點從IGMH圖上就可以明顯看出來,即C60@2C34中綠色的兩條環狀等值面明顯比C60@2C30的窄很多。這體現出恰當利用IGMH方法可視化分子間相互作用,甚至可以把不同體系間輕微的差異性也給明確揭示出來。《直觀解釋分子間相互作用如何影響不對稱催化:Nature Chemistry上一個很好的IGMH分析范例》(http://www.shanxitv.org/700)里的例子也同樣體現了這一點。
各個片段在結合成C60@2Cn三聚體過程中的總變形能如上圖的黑線所示,由于富勒烯的剛性很強,因此變形能基本都來自于碳環的變形。可見隨著碳環的增大,變形能也逐漸上升,這在于越大的碳環柔性越強。從前面的結構圖甚至肉眼都能明顯看出來C30碳環在三聚體結構中有明顯的彎曲。而C34的變形能則小于C30,這是因為C60@2C34復合物中的兩個C34基本是圓形、平面的結構,和孤立狀態結構特征相差較小,而且此結構中C34與富勒烯的相互作用沒有C30的那么強。
3 碳環-富勒烯 1:2三聚體
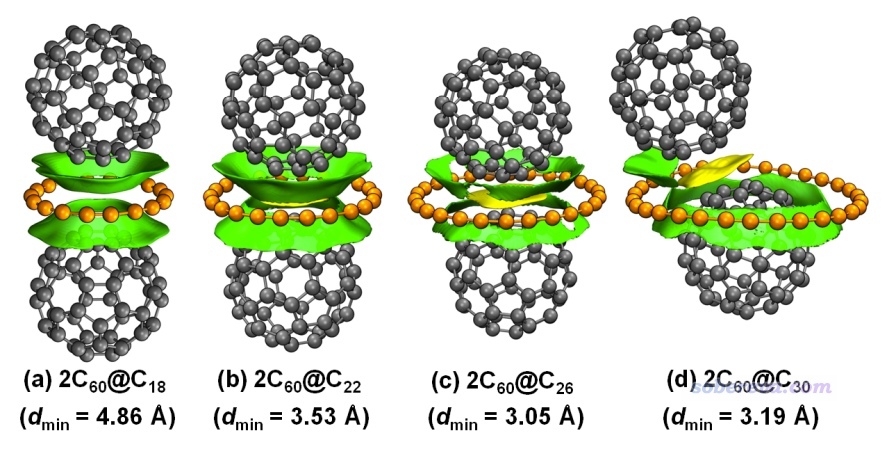
下面再來看一個碳環與兩個富勒烯結合成2C60@Cn(n=18到30)三聚體的情況。優化后的復合物結構和IGMH圖如下所示,綠色等值面展現富勒烯與碳環之間的相互作用,黃色等值面展現兩個富勒烯之間的相互作用。標注的d_min對應兩個富勒烯之間最近原子距離(可以將結構文件載入Multiwfn,進入主功能100的主功能21,輸入dist,然后依次輸入兩個片段里的原子序號得到此值)。由圖可見,從C18到C26碳環,碳環越大,由于對兩個富勒烯之間的接觸阻礙越小,富勒烯之間的距離越近、富勒烯之間的相互作用越顯著。碳環從C22變成C26時,富勒烯與碳環之間的IGMH等值面明顯變窄,體現相互作用明顯變弱,和富勒烯之間的相互作用強度的變化形成了此消彼長的關系。對于2C60@C30的情況,碳環與兩個富勒烯的相互作用不再對稱,上面的富勒烯歪到一側去了,與碳環的相互作用顯著小于下面的富勒烯,因此可以預料2C60@C30的穩定性明顯不及2C60@C26。
下圖(a)給出了2C60@Cn的三聚體總結合能(黑線),以及結合第一個和第二個富勒烯時候的結合能(紅線和藍線)。可見碳環越大,對第一個富勒烯的結合越強,這在前文的碳環-富勒烯二聚體的研究中已經說過。由于已有的富勒烯會對第二個結合的富勒烯產生吸引作用,對于2C60@C18、2C60@C22、2C60@C26,第二個富勒烯的結合能比第一個富勒烯的結合能更負,即兩個富勒烯與C18、C22、C26碳環的結合有明顯的協同效應。而對于2C60@C30,由于第一個富勒烯嚴重妨礙第二個富勒烯的結合,導致第二個富勒烯只能歪斜著與C30碳環發生較弱的相互作用,同時第二個富勒烯結合時還稍微削弱了第一個富勒烯與碳環的相互作用,因此第二個富勒烯的結合能只有第一個富勒烯結合能的一半。
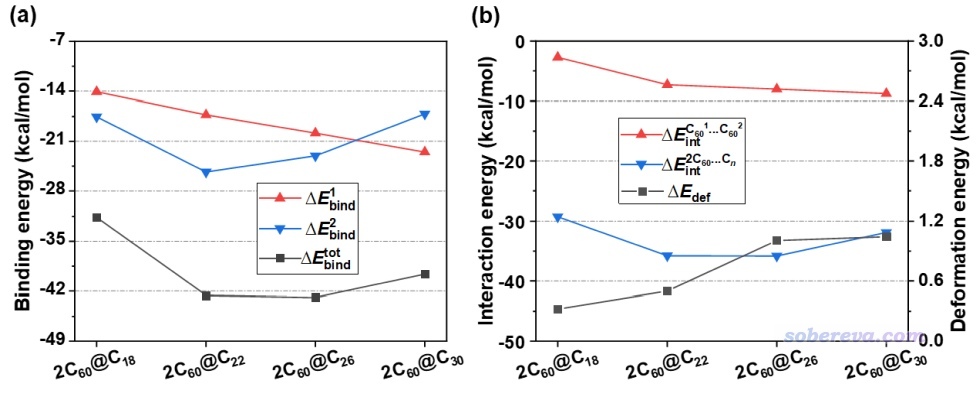
上圖(b)更進一步考察了2C60@Cn的三聚體中各個片段間的相互作用能。可見由于碳環越大、越不給富勒烯之間的接觸礙事,圖中紅線對應的富勒烯之間的相互作用能是隨著碳環的增大而越來越負的。圖中藍線體現C22和C26與兩個富勒烯的相互作用最強,而C30由于只能松散地與其中一個富勒烯相互作用,因此它與兩個富勒烯的總相互作用更弱一些。
根據以上信息,文中提出了新穎的“分子膠水”的概念。大小恰到好處的碳環,如C22,可以把兩個富勒烯特別牢固地粘在一起。C22對第二個富勒烯的結合能,也等價于C60@C22與一個富勒烯的結合能,達到了約-42 kcal/mol,這比起兩個富勒烯之間的結合能-8.3 kcal/mol強太多了,甚至都輕微超過了C-C單鍵鍵能的一半!!!
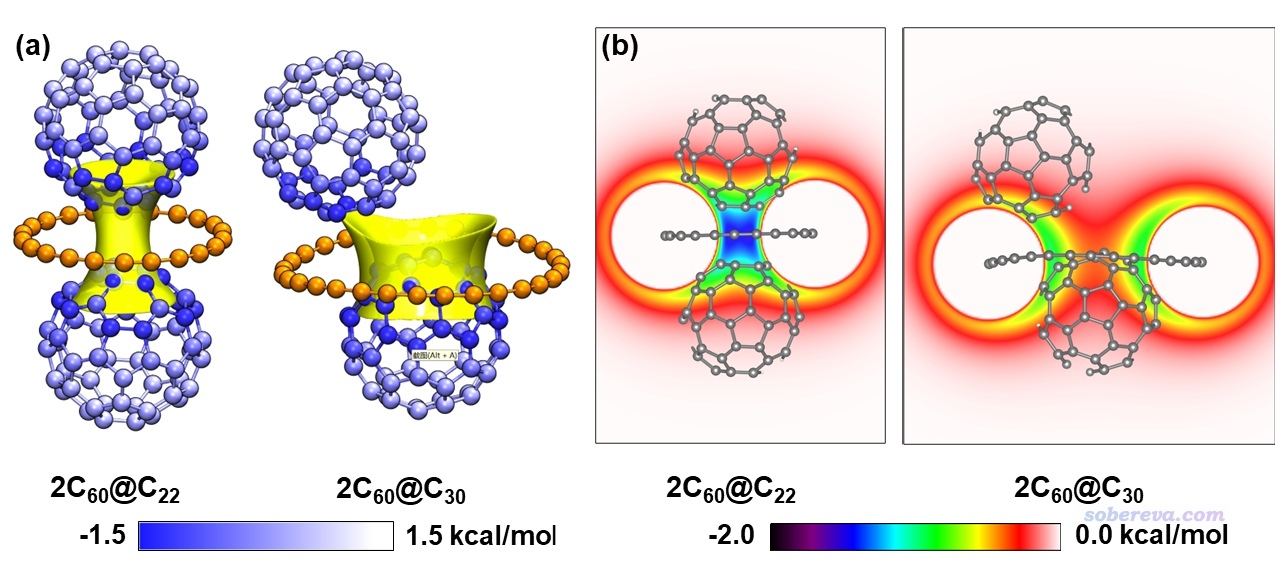
為了更充分地探究碳環對富勒烯結合起到的膠水作用,此文運用了《談談范德華勢以及在Multiwfn中的計算、分析和繪制》(http://www.shanxitv.org/551)中介紹的方法,基于GAFF力場參數繪制了2C60@C22和2C60@C30三聚體結構中碳環產生的范德華勢,以碳原子為探針原子,如下所示。圖(a)的黃色等值面對應范德華勢=-0.8 kcal/mol,富勒烯的原子按照原子所在位置的范德華勢著色,顏色越藍體現富勒烯的相應原子與碳環間的色散吸引作用越強。圖(b)是利用VESTA程序基于Multiwfn產生的范德華勢cube文件繪制的填色平面圖。由圖可見C22碳環的范德華勢最負的區域從碳環中心向上下兩側延伸出來,沒過了每個富勒烯大約1/3的區域,顯然C22碳環的這種范德華勢分布能恰到好處地把兩個富勒烯粘起來,是富勒烯之間最簡單且最完美的膠水分子!而碳環也不宜過大,如圖中C30的情況,雖然其范德華勢很負的區域能覆蓋下方的富勒烯將近一半的原子,但對上方的富勒烯的色散吸引則較為有限。盡管如此,C30對第二個富勒烯的結合能-17.1 kcal/mol仍然比兩個富勒烯之間的結合能-8.3 kcal/mol負得多。因此哪怕碳環偏大,照樣能促進兩個富勒烯的結合。
4 一個富勒烯最多能結合多少個18碳環?
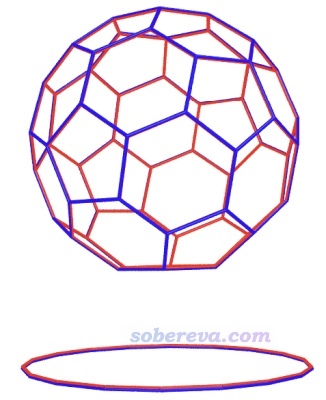
從前面給出的兩個18碳環與一個富勒烯形成的復合物來看,富勒烯表面實際上還有空間可以結合更多的18碳環。那么一個富勒烯最多能結合多少個18碳環?多少個碳環才能令富勒烯的表面飽和?為了探究這個有趣的問題,文中根據碳環和富勒烯的結構,搭建了6個碳環均勻分布在富勒烯上下左右前后的結構并做了幾何優化。由于此體系多達168個碳原子,用ωB97XD/6-311G*優化和振動分析實在過于昂貴,所以這部分的計算對碳環用6-311G,而對富勒烯用6-31G。這么做的合理性一方面在于碳原子對于極化函數的要求遠低于雜原子,另一方面是以C60@C18進行測試,6-311G&6-31G優化的結果與6-311G*的結果的差異確實可忽略不計,分別如下圖的紅線和藍線所示(原文圖S4),可見幾乎完全重合。注意18碳環的基組不能再減小到6-31G,這點筆者在《我對一篇存在大量錯誤的J.Mol.Model.期刊上的18碳環研究文章的comment》(http://www.shanxitv.org/584)中專門指出過。
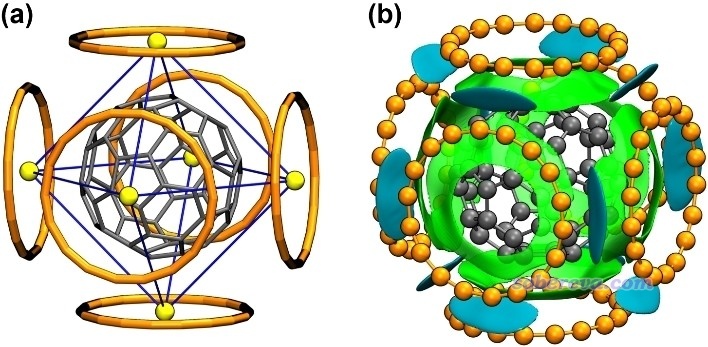
優化得到的富勒烯結合6個18碳環的結構如下圖(a)所示。為了清楚起見,在VMD程序里通過繪圖命令用黃色圓球把18碳環中心位置顯示了出來,并且把相鄰的黃球用藍線連了起來,由此可以清楚地看出6個碳環構成了一個包圍富勒烯的近乎理想的正八面體空間。下圖(b)是IGMH圖,依然是富勒烯與碳環之間的作用用綠色展示,碳環之間的作用用青色展示,可見這個C60@6C18結構中每個碳環都與富勒烯產生了非常顯著、充分的pi-pi作用,而且每一對相鄰碳環之間也產生了特別顯著的pi-pi作用,這是何等完美的結構啊!6個18碳環與富勒烯的結構匹配程度完美到令人驚嘆!
在ωB97M-V/def2-TZVP+gCP級別下計算的C60@6C18的總結合能高達-101.3 kcal/mol,已經達到了常規化學鍵的數量級!此體系中平均每個18碳環的結合能是-101.3/6=-16.9 kcal/mol,這比起C60@2C18中18碳環平均結合能-15.0 kcal/mol更負,體現出C60@6C18的形成過程的協同作用真是巨強。這在于此體系中每個18碳環都能同時與周圍四個18碳環充分地吸引。C60@6C18在氣相標況下的結合自由能為-13.4 kcal/mol,體現出此結構在熱力學上很容易自發形成。
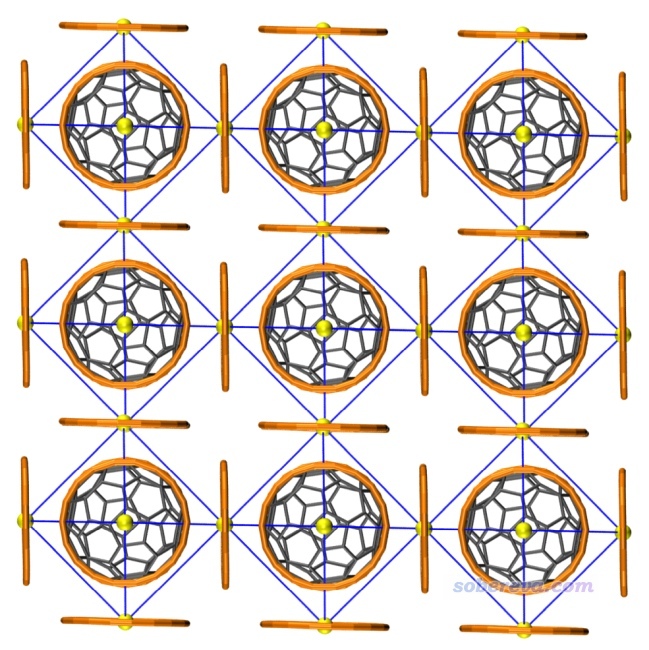
基于C60@6C18的結構,文章還大膽地設想了富勒烯與18碳環形成的共晶的結構,示意圖如下所示(原文圖S4)。此結構里每個碳環、富勒烯都最大程度利用了自己的色散吸引能力與對方結合,因此應當是一個頗為穩定、大概率在未來能被實驗合成出來的晶體。
5 總結
本文介紹的Chem. Eur. J., 30, e202402227 (2024)一文通過嚴謹的量子化學計算并充分運用Multiwfn實現波函數分析,首次預測了各種尺寸碳環與不同數目C60富勒烯形成的復合物的結構,并深入探討了相互作用強度和本質。此文體現出富勒烯與碳環這兩種碳的同素異形體之間通過pi-pi作用表現出極強的親合性。碳環體系以其特殊的環形幾何結構以及獨特的兩套全局共軛的pi電子,還可以作為分子膠水將兩個富勒烯牢牢粘在一起。文章還證明了一個富勒烯最多能結合6個18碳環,而且結合過程中有顯著的協同性,結合越多越容易。因此靠富勒烯吸附碳環,或許在未來能成為一種富集富勒烯的手段。文章還預測了富勒烯與18碳環形成共晶的可能,在未來有可能能以這種形態將不穩定的18碳環穩定地儲存起來。
此文是通過理論計算研究新穎的分子間復合物的很好的例子,兼具重要的理論意義和實際意義。同時此文也是利用Multiwfn做波函數分析探究弱相互作用的很好的范例,把相互作用特征研究得十分通透,尤其是IGMH方法把富勒烯與碳環的復合物中的弱相互作用展現得超級生動直觀、一目了然,此文充分體現出掌握Multiwfn程序做波函數分析對弱相互作用研究的關鍵性價值!
另外,如果你對pi-pi研究感興趣,強烈建議閱讀《談談pi-pi相互作用》(http://www.shanxitv.org/737)。