談談質子轉移、氫原子轉移、氫負離子轉移的關系
談談質子轉移、氫原子轉移、氫負離子轉移的關系
文/Sobereva@北京科音
First release: 2021-Dec-23 Last update: 2022-Jul-29
0 前言
質子轉移、氫轉移、氫負離子轉移是關系密切相關的三個化學過程,有時候有人問相關的問題。我覺得有必要寫一個小文總結一下它們的差異,使讀者能分清它們的關系。與此同時筆者還會從量子化學波函數分析角度提及一些相關的問題,給我的一些觀點,以助于量子化學研究者正確地認識這些過程的本質。
1 質子轉移(Proton Transfer)
質子轉移本意是一個質子(不帶電子的氫原子核)的轉移。可以在離子間,也可以在中性物質間。可以在不同體系間,也可以在同一個體系內。
1.1 離子間質子轉移
離子間(至少二者其中一方是離子)質子轉移常見的情況有以下這些(孤對電子用:來凸顯。離子用括號表示)
? 陽離子向中性分子轉移:(A-H)+ + :B → A: + (H-B)+
? 陽離子向陰離子轉移:(A-H)+ + (:B)- → A: + H-B
? 中性向陰離子轉移:A-H + (B)- → (A:)- + H-B
直接根據轉移前后物質的帶電情況就能判斷是不是質子轉移。比如酸性條件催化乙酸乙酯水解的過程中,第一步是質子化的水(H3O)+將質子向乙酸乙酯的氧轉移。
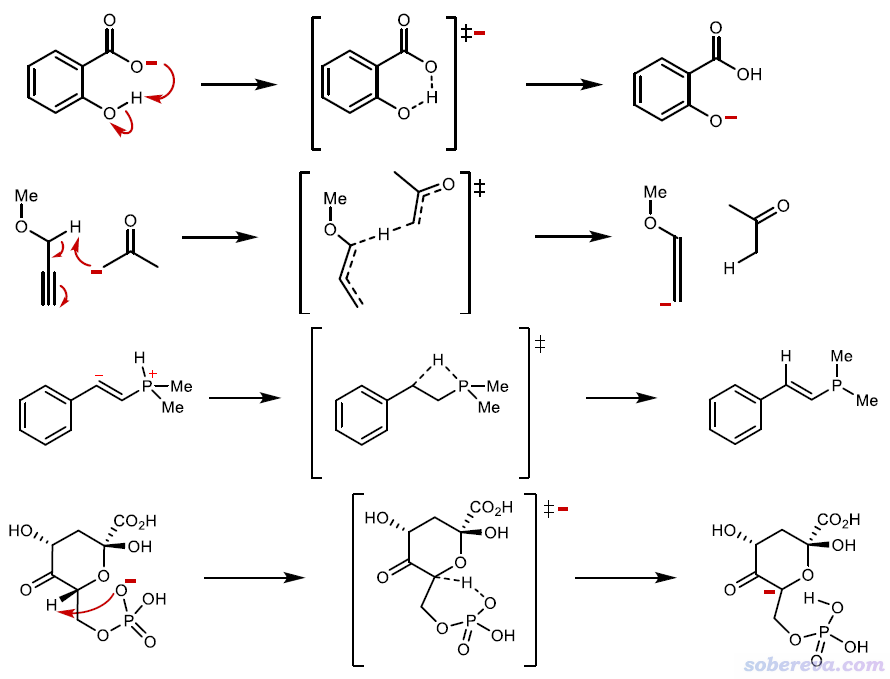
以下是其它離子間(或同一個物質的局部顯離子性片段間)的質子轉移例子。取自DOI: 10.1021/acs.jctc.1c00694的SI。
1.2 中性間質子轉移
中性間的質子轉移形式有
? 轉移之后還是中性:A-H + :B → A: + H-B
? 轉移之后成為陽離子和陰離子:A-H + :B → (A)- + (H-B)+
注意,接受H和給H的對象,即A和B上會與H連接的原子,都應當是電負性較大的原子,這樣轉移的H才顯著帶正電荷,才基本算得上質子。這種情況下,A-H...B在形式上可以被算作是氫鍵(但未必轉移過程的各個幾何結構下都能滿足氫鍵判據)。
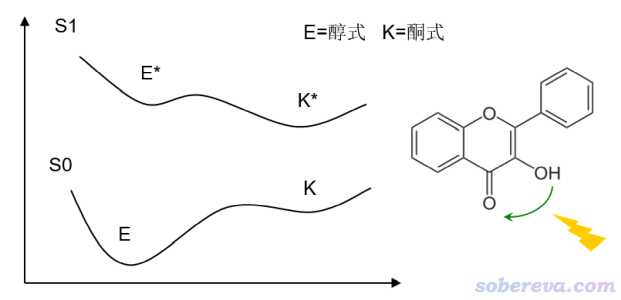
下面是典型的能發生分子內A-H + :B → A: + H-B型質子轉移的體系,3-羥基黃酮。在基態和激發態勢能面都可以發生對應醇式->酮式變化的質子轉移,但在激發態勢能面下無論是動力學上還是熱力學上都明顯更容易發生,這稱為激發態分子內質子轉移(excited-state intramolecular proton transfer, ESIPT)。
在高極性溶劑下,氨基酸上的-COOH會向-NH2自發發生質子轉移成為-COO-和-NH3+;在水中硫酸會向水質子轉移成為[HSO4]-和H3O+,都是典型的A-H + :B → (A)- + (H-B)+的質子轉移情況。
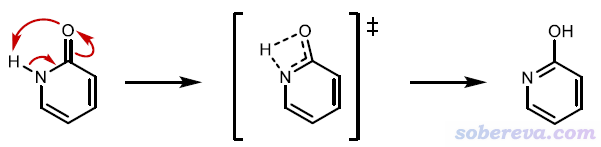
下面是2-pyridone向2-hydroxypyridine的異構化。由于給H和受H的分別是N和O,電負性都很大,因此姑且稱得上是質子轉移。N-H...O也是典型的氫鍵形式,雖說在初始結構下由于氫鍵鍵角太大因此還稱不上是氫鍵。
下面是水輔助的質子轉移的例子。雖說H也不是不能從N直接遷移到O上去,但借助水實現質子轉移明顯勢壘低得多。
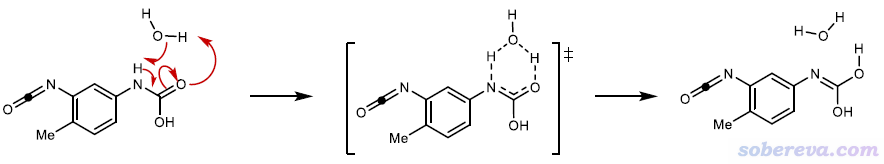
在這一節最后特別要強調的一點是,現實當中,質子轉移過程絕對不是真的像字面意思那樣,一個一丁點電子都不帶的質子發生轉移!對于前面的那些例子,無論對反應物、過渡態還是產物去計算H的各種形式的原子電荷(ADCH、NPA、CHELPG...,不懂的話看《原子電荷計算方法的對比》http://www.whxb.pku.edu.cn/CN/abstract/abstract27818.shtml),H的原子電荷都只有零點幾而已,即轉移的微觀過程中質子上始終附著著不少電子。如果跑IRC或者做一個從頭算動力學模擬,也沒有哪一幀結構H帶的原子電荷恰好是+1,即完全是質子狀態。例如下面是2-pyridone向2-hydroxypyridine的質子轉移對應的異構化過程的過渡態,在M06-2X/6-31G**級別下對轉移的H10通過Multiwfn程序用流行的ADCH、Hirshfeld、Mulliken、CHELPG、Hirshfeld-I方法算的原子電荷分別是0.195、0.143、0.372、0.303、0.412,雖然定量上有所不同但都遠小于H只含一個質子時對應的原子電荷1.0。
還要強調的是,上面的一些Lewis式里面的完全定域化形式的電子結構很大程度上和真實電子結構不符。例如第一張圖里COO-把負電荷只標在了一個氧上,但實際上對優化后的反應物去計算原子電荷,兩個氧的原子電荷相差并不很大,即額外的負電荷是離域在兩個氧上的。關于這一點后面還會看到例子。
2 氫原子轉移(Hydrogen Atom Transfer, HAT)
氫原子轉移也相當于氫原子抽取(Hydrogen-Atom Abstraction, HAA)過程,通常形式為A-H + ?B → A? + H-B。這種轉移強調轉移過去的是氫原子,即質子和電子是協同轉移的。一般接受氫原子的物質是自由基。和中性分子間的質子轉移還有個不同點是A、B不需要都是電負性比較大的原子。接受氫原子的也不非得是自由基。比如Eur. J. Org. Chem., 2017, 2056 DOI: 10.1002/ejoc.201601485這個綜述里介紹了光催化劑被光激發后也可以作為抽氫的物質。
下面是一些氫原子轉移的典型例子
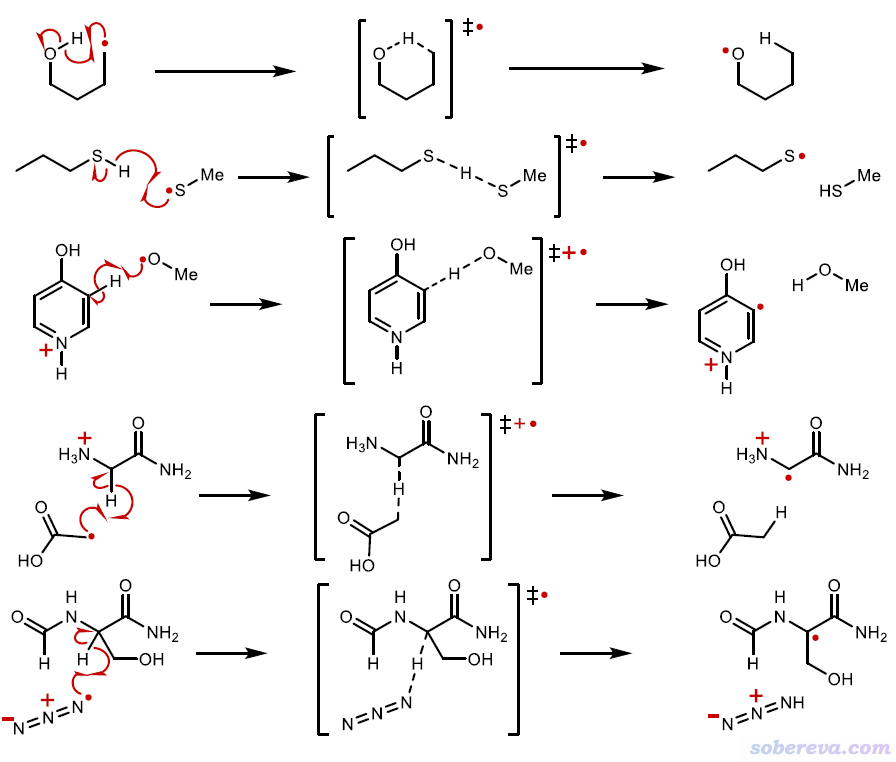
判斷是不是分子間氫原子轉移的關鍵依據就是看轉移后是不是接受H的一方電子數增加了1,只要知道反應物和產物是什么自然就能判斷。對于判斷是不是分子內的氫原子轉移,可以對過渡態結構計算給H和受H的原子的自旋布居(做法看《談談自旋密度、自旋布居以及在Multiwfn中的繪制和計算》http://www.shanxitv.org/353),如果都明顯大于0,就算得上是氫原子轉移。例如下圖是H + CH4 → H2 + CH3的抽氫反應的過渡態結構和Multiwfn程序對B3LYP/6-31G**波函數用Hirshfeld方法算的原子自旋布居,可見兩個原子的數值都明顯大于0,故是典型的氫原子轉移過程。
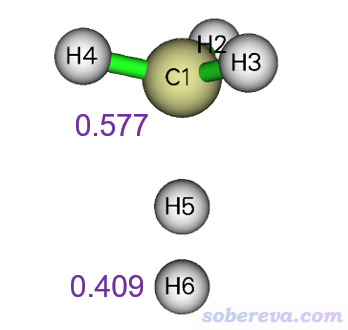
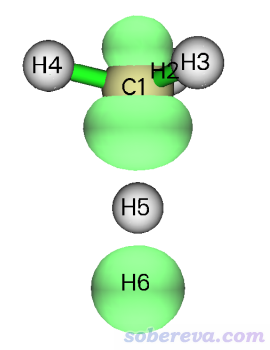
還需要提醒的是,不要以為氫原子轉移在微觀機制上是一個一般形態的氫原子轉移過去的。一個孤立存在的氫原子是一個原子核帶一個未成對電子,原子電荷為0、自旋布居為1。如果是一般形態的氫原子發生轉移,在過渡態的時候自旋布居就算達不到理想的1,至少也肯定是顯著大于0的數值。但事實上,轉移的氫原子可以帶著近乎等量的alpha和beta電子,即幾乎沒有單電子。例如上面的例子,過渡態結構下用Multiwfn畫的0.02 a.u.等值面數值的自旋密度圖如下,綠色代表正值等值面。可見在轉移的H5上等值面沒有分布,其Hirshfeld原子自旋布居也基本為0,而其Hirshfeld原子電荷卻幾乎為0,體現出在這個原子上同時有大約0.5個alpha和0.5個beta電子。
3 氫負離子轉移(Hydride Transfer)
氫負離子轉移,可以為A-H + (B)+ -> (A)+ + H-B,可見H轉以后令B那部分不帶電了,因此可以認為轉移過去的是個氫負離子(氫上帶了兩個電子)。也可以為(AH)- + B -> A + (HB)-,形式上H帶了一個額外負電荷過去。下面是一些具體例子。注意在這個轉移過程中,如果用量子化學方法考察,并不會發現H上帶明顯負電,畢竟H的電負性很小,因此事實上只不過是隨著H的轉移,電子從A大量流到B上而已。
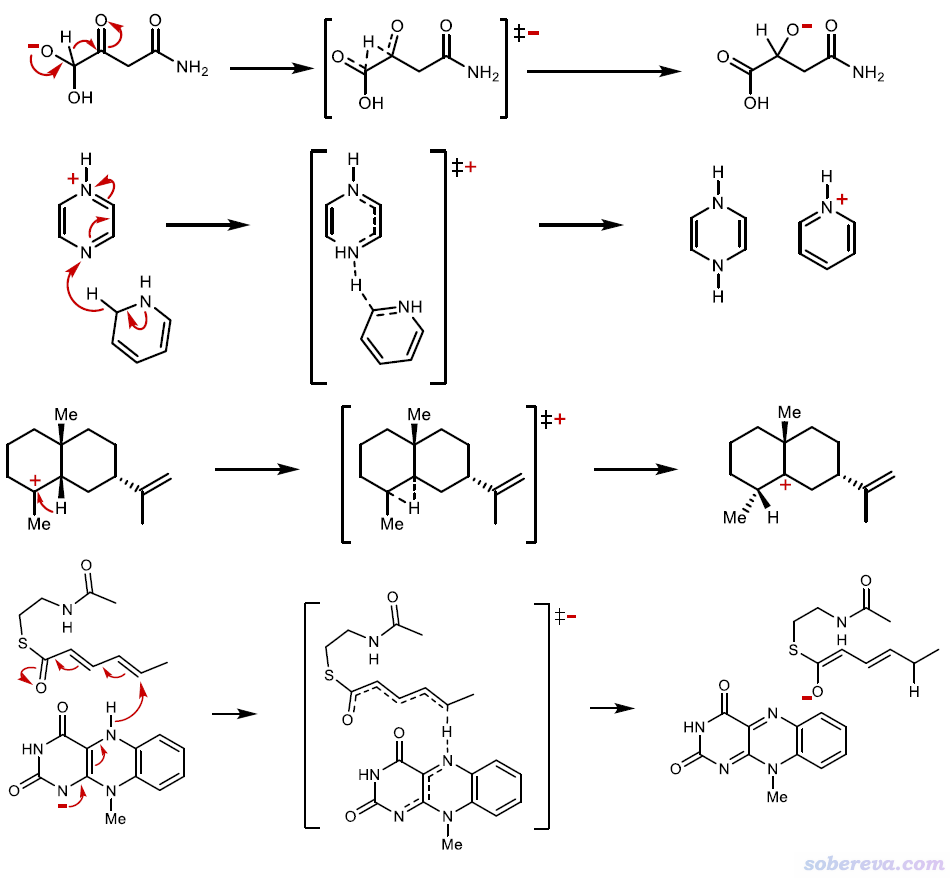
再強調一下,前面那些Lewis圖描述的電子結構很多都是極不確切的。尤其是分子內氫負離子轉移,其實只能算得上是“Lewis式變化角度上的氫負離子轉移”。如果脫離了Lewis式,從嚴格的量子化學角度看待,其實說是氫負離子轉移是極度牽強的。比如上圖第一個反應式,其反應物(R)、過渡態、產物(P)的結構圖如下,幾個氧原子以及轉移的H的Mulliken和ADCH原子電荷分別用紫字和綠字標注了
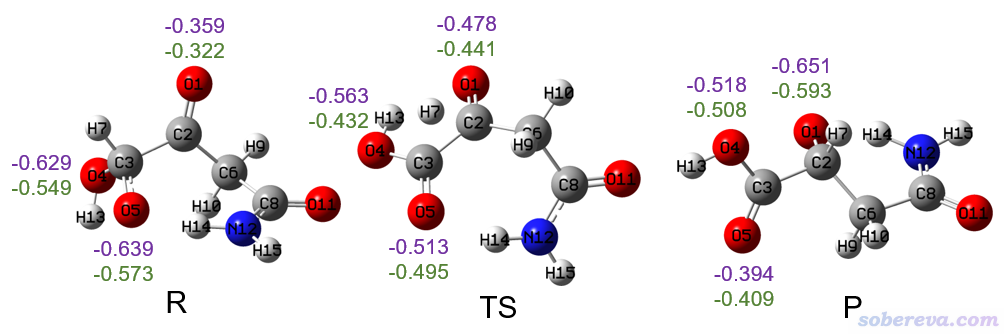
按照前面的反應式,隨著H7的遷移,O5上的一個形式負電荷將會完全轉移到O1上。但事實上,從上面圖中的原子電荷來看,電子的轉移遠遠遠遠沒有這么夸張。反應物結構下,O5和O4帶的負電荷是基本一樣多的,在產物結構下,O1帶的負電荷也沒比O4多多少,所以簡單認為這個陰離子體系的負電荷只會集中分布在某個氧上是荒謬的。另外,H遷移前后,O5的ADCH電荷從-0.573變為-0.409,改變了+0.164;O1的ADCH電荷從-0.322變為了-0.593,改變了-0.271。無論從哪一方的原子電荷變化來看,在H轉移過程中從O5向O1凈轉移的電子都遠遠遠遠達不到1。另外,轉移過程中H的帶電量也基本沒變化。所以,上例的情況其實只能算得上是有那么一些氫負離子轉移的特征罷了,僅當(裝傻地、自我欺騙地)把電子結構的定域性夸張描述到Lewis式所表現的程度(而且不考慮Lewis式之間的共振),才能說成是本格的氫負離子轉移!至于前面給出的各種反應式里的彎箭頭,有的還多多少少有那么一點合理性、能多多少少稍微體現一些電子轉移的實際情況,而有的真的就是隨意地人為臆測、定性都是錯的,因此切勿太當回事。
4 其它情況
最后再提一下,絕對不要但凡看見H的轉移的反應,就非得把它歸屬于質子轉移、氫原子轉移、氫負離子轉移中的一種,尤其是分子內的H轉移。比如說HCN→CNH的異構化反應,說它是質子轉移,顯得不科學。因為如果非要這么說的話,用Lewis式來表達,是從H-C≡N變成(C-)≡(N+)-H,但(C-)≡(N+)-H的描述對于CNH來說很不合理,實際算出來的原子電荷和此Lewis式所示意的情況大相徑庭,因此稱為質子轉移明顯不合適。而若說它是氫原子轉移,和一般的氫原子轉移的情況相比,這反應又沒體現出轉移前后單電子主要分布位點發生改變,況且本來轉移全過程都是閉殼層狀態,連單電子都沒有。此反應也更是一點氫負離子轉移的特征都沒有。所以像這種反應,就簡簡單單地籠統說成“氫轉移”就完了,而不要去強行去聲明轉移的具體形式和氫的形態。
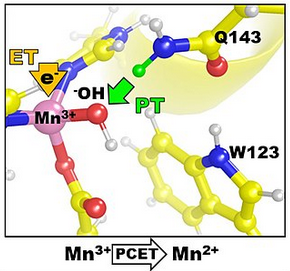
還有一種轉移叫質子耦合電子轉移(Proton-coupled electron transfer, PCET),是指電子和質子協同發生轉移。這表面看起來好像和HAT轉移似的,HAT轉移的氫原子不就是一個質子帶一個電子么?PCET之所以有一個專門的詞,是強調轉移的質子和電子始于不同的位點,而且去往不同的位點。例如下面的圖就是一個例子,Q143氨基酸殘基的質子往帶負電的OH配體部分轉移,與此同時,電子往Mn(III)上轉移。