比SMD算溶解自由能更好的溶劑模型uESE的使用
比SMD算溶解自由能更好的溶劑模型uESE的使用
文/Sobereva@北京科音 2021-Apr-30
1 uESE溶劑模型簡介
SMD是如今非常常用的溶劑模型,在《談談隱式溶劑模型下溶解自由能和體系自由能的計算》(http://www.shanxitv.org/327)里筆者專門介紹過。在Gaussian程序中,SMD的極性部分等同于IEFPCM,而由于其非極性部分考慮較周到,因此溶解自由能計算精度較好。但是SMD算離子體系的溶解自由能誤差遠大于算中性體系的,通常需要用顯式+隱式的雜化溶劑模型才能得到較好結果。
最近Vyboishchikov等人提出了uESE (universal Easy Solvation Energy Evaluation)溶劑模型,原文見J. Comput. Chem. (2021) DOI: 10.1002/jcc.26531。之前還有xESE溶劑模型,和uESE形式很相似,原文見Phys. Chem. Chem. Phys., 22, 14591 (2020)。uESE/xESE都像SMD一樣考慮了溶質-溶劑相互作用的極性和非極性部分,但uESE/xESE和SMD有很大不同:
(1)uESE/xESE的極性部分利用的是COSMO模型。通常COSMO是基于電子密度計算的,而是uESE/xESE的COSMO則是基于CM5原子電荷計算的;更具體來說,在求解表面顯著電荷時利用使用CM5電荷計算溶質孔洞表面的靜電勢。
(2)uESE/xESE模型并不納入SCF迭代過程中,也不影響電子結構,不能計算帶溶劑模型時的受力和Hessian,相當于是一個“后”溶劑模型。uESE/xESE僅適合基于CM5電荷算溶解自由能的目的。由于uESE/xESE中的參數是基于氣相下B3LYP/def2-TZVP級別的結構和波函數計算的CM5原子電荷擬合的,所以自己用uESE/xESE的時候CM5電荷也得在這個級別下計算。
(3)uESE/xESE包含對溶劑-溶質極性作用部分的經驗校正項。
(4)uESE/xESE對于不同類型溶劑使用不同的極性部分的校正項和非極性部分形式。溶劑分為四類:水,非水極性質子溶劑,極性非質子溶劑,非極性溶劑。
(5)uESE/xESE擬合的經驗參數中既有依賴于元素的,也有依賴于溶劑類型的,也有依賴于溶劑本身的。目前xESE只支持水,uESE支持約100種溶劑。極性部分校正項和非極性部分只有H,C,N,O,F,P,S,Cl,Br,I元素的參數(對于其它元素只能給出COSMO極性部分的結果)。而SMD不含依賴原子半徑以外元素的參數。
uESE和xESE有什么存在意義?主要意義在于算溶解自由能從統計結果上比SMD更好,特別是對于離子體系。根據uESE原文的測試,溶解自由能計算精度(平均絕對誤差,MAE)有下面的關系
中性體系:xESE≈SM12>=uESE>=SMD
陽離子體系:uESE>xESE>SMD>=SM12
陰離子體系:uESE>xESE≈SMD12>>SMD
即曰,算中性體系溶解自由能,用xESE會比SMD占一點優勢。算陽離子用uESE比用SMD強得多。算陰離子更是絕對不能直接用SMD,不想用雜化溶劑模型的話至少也應當用uESE。根據測試,uESE算中性體系溶解自由能的MAE小于1 kcal/mol,算陰、陽離子溶解自由能的MAE差不多,都小于3 kcal/mol。而SMD算陰離子的MAE則達到8 kcal/mol左右。注:上面的SM12和SMD是同門的,但前者和uESE一樣也是基于CM5原子電荷進行計算,不過極性部分利用的是廣義Born方程形式。
下圖左側是uESE原文里算大量中性和離子在非水質子溶劑中的溶解自由能(縱坐標)與實驗值(橫坐標)的對比,右圖是SMD算的情況,誤差超過4 kcal/mol的用紅色符號高亮。可見uESE算中性溶質的情況比SMD稍好,而計算離子的情況能好很多。
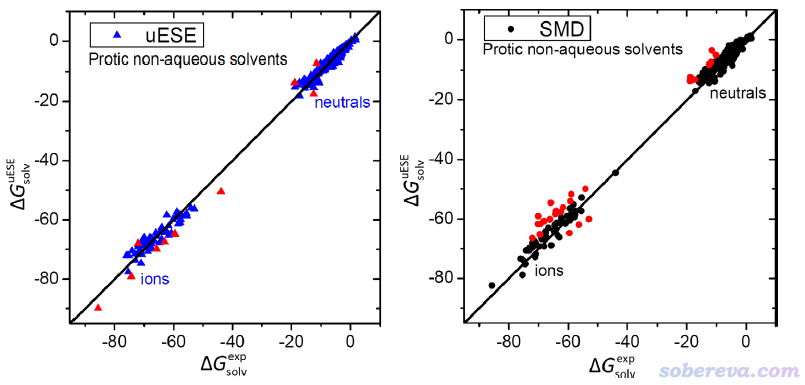
下圖是計算在極性非質子溶劑中的溶解自由能的情況。可見此時SMD算離子的情況表現極差,特別是對于溶解自由能非常大的離子
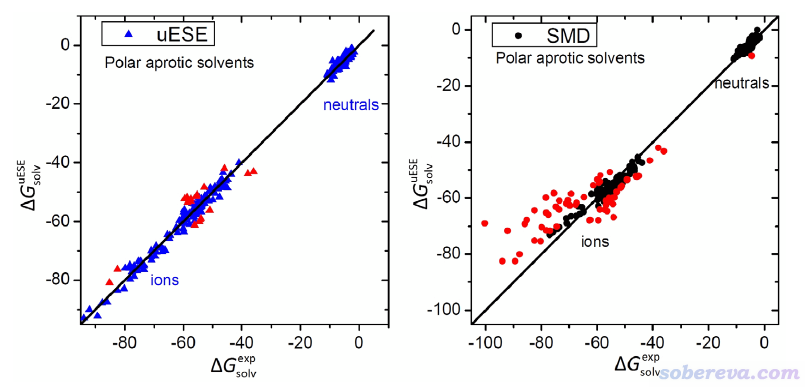
需要注意的是以上都是統計數據,大家也不要指望算每個中性體系xESE都比SMD好、算每個離子體系uESE都一定比SMD好。筆者寫此文的目的主要是提醒大家算離子體系的溶解自由能的時候,如果懶得用雜化溶劑模型,則至少要用uESE,切勿拿SMD湊合(除非有uESE不支持的元素)。
2 uESE和xESE程序的使用
uESE和xESE方法有同名的計算程序,可以在http://iqcc.udg.edu/~vybo/ESE/直接下載,Windows和Linux版可執行文件都提供了,不開源。這兩個程序用的輸入文件相同,uESE可以指定溶劑,而xESE只支持水溶劑。
uESE和xESE都需要基于命令行使用。uESE在Windows下的使用格式是:uESE.exe [輸入文件路徑] -solvent [溶劑名]。可以用的溶劑見http://iqcc.udg.edu/~vybo/ESE/solvent-list.html。
uESE/xESE的輸入文件里需要提供各原子的元素在周期表里的序號、原子坐標,以及原子的CM5電荷。筆者開發的Multiwfn波函數分析程序(主頁&免費下載:http://www.shanxitv.org/multiwfn)直接就能計算CM5電荷。為了令用戶能盡可能方便地產生uESE/xESE的輸入文件,從2021-Apr-30更新的Multiwfn開始只要將settings.ini里的uESEinp參數設為1,則Multiwfn計算完CM5電荷后就會問你是否產生uESE/xESE的輸入文件。使用uESE/xESE算溶解自由能用的輸入文件若是Multiwfn產生的,請注意在你發表的文章中提及,并按照Multiwfn啟動時的提示恰當引用Multiwfn。
Multiwfn計算CM5電荷需要提供含有波函數的信息作為輸入文件,諸如.wfn/.wfx/.fch/.molden/.mwfn等等,產生方式見《詳談Multiwfn支持的輸入文件類型、產生方法以及相互轉換》(http://www.shanxitv.org/379)。不了解Multiwfn的話參看《Multiwfn FAQ》(http://www.shanxitv.org/452)。
3 使用uESE計算PhO-在乙腈中的溶解自由能實例
下面就通過一個例子演示uESE程序的使用,是PhO-(苯酚的羥基的質子解離掉后的陰離子)在乙腈中的溶解自由能計算。此例所有相關文件可以在http://www.shanxitv.org/attach/593/file.rar下載。本例Gaussian使用G16 A.03版,Multiwfn是2021-Apr-30更新的3.8(dev)版,操作系統是Win 10 64bit。
首先用Gaussian對PhO-進行優化。根據uESE原文,應當用B3LYP/def2-TZVP在真空下進行。輸入文件如下
%chk=C:\PhO-_optfreq.chk
#p B3LYP/def2TZVP opt freq
[空行]
Title Card Required
[空行]
-1 1
C 0.00000000 0.00000000 -1.80531390
C 0.00000000 -1.20821014 -1.10754617
C 0.00000000 -1.20820376 0.28716582
C 0.00000000 0.00000000 0.98475086
C -0.00000000 1.20820376 0.28716582
C -0.00000000 1.20821014 -1.10754617
H 0.00000000 0.00000000 -2.90492418
H 0.00000000 -2.16044049 -1.65754504
H 0.00000000 -2.16042940 0.83722286
H -0.00000000 2.16042940 0.83722286
H -0.00000000 2.16044049 -1.65754504
O 0.00000000 0.00000000 2.41475076
計算完成后,檢查輸出文件確認沒有虛頻。然后用formchk將PhO-_optfreq.chk轉換為PhO-_optfreq.fch。formchk的使用在《詳談Multiwfn支持的輸入文件類型、產生方法以及相互轉換》(http://www.shanxitv.org/379)里說了。
將Multiwfn目錄下的settings.ini里的uESEinp設為1,然后啟動Multiwfn,載入PhO-_optfreq.fch,之后依次輸入
7 //布居分析與原子電荷計算
16 //計算CM5電荷
1 //使用內置的球對稱化的自由原子密度
[按回車] //產生的uESE輸入文件為當前目錄下的PhO-_optfreq.inp
然后就可以把Multiwfn窗口關了。
下載uESE的Windows版可執行文件uESE.exe到某處,把PhO-_optfreq.inp放到與此文件相同的目錄下,然后按Win+R鍵,輸入cmd進入命令行界面,通過cd命令進入此目錄下(這種計算機基本常識不會的話自行Google),運行uESE PhO-_optfreq.inp -solvent acetonitrile。僅需一秒鐘就能運行完,在輸出信息中會看到
COSMO electrostatic energy = -66.946 kcal/mol
Correction term = 12.393 kcal/mol
Total solvation free energy = -54.554 kcal/mol
即曰溶解自由能是-54.554 kcal/mol。uESE/xESE給出的溶解前后都是1M濃度的溶解自由能。從SMD溶劑模型原文的補充材料里可以查到實驗值是-55.1 kcal/mol(也是溶解前后都是1M的情況),可見此例uESE表現得極為理想,誤差僅有0.55 kcal/mol,不過這很大程度上是運氣好。
下面也用SMD模型算一下溶解自由能,做法在《談談隱式溶劑模型下溶解自由能和體系自由能的計算》(http://www.shanxitv.org/327)里專門講過。基于上面B3LYP/def2-TZVP氣相下優化的結構,在M05-2X/6-31G*級別下算一次氣相單點能和SMD模型表現的乙腈環境下的單點能,結果為
# M052X/6-31G* scrf(SMD,solvent=acetonitrile):-306.941786445 Hartree
# M052X/6-31G*:-306.847792107 Hartree
因此溶解自由能為627.51*(-306.941786445+306.847792107)=-58.98 kcal/mol。相對于實驗的誤差達到-3.9 kcal/mol,明顯大于uESE的,這體現出了uESE的顯著優勢。
注意uESE模型在測試、擬合參數的時候對離子體系都是只考慮了帶+1、-1電荷的離子。高價離子與溶劑相互作用顯著強于一價離子,筆者估計用uESE肯定不會得到較好結果,必須用雜化溶劑模型。